Misforståelse eller bevisst feilinformasjon om biomedisiner?
Kan utformingen av TNF/BIO-dokumentet til Sykehusinnkjøp føre til at leger i klinisk praksis tror at noen biologiske produkter ikke lenger kan forskrives? Teorien var plutselig der, og magefølelsen sa til journalisten i meg at det var viktig å snuse videre for å finne svar.
Det er ingen tvil om at det finnes en rekke forskningsstudier som viser at bytte mellom biotilsvarende legemidler fungerer godt for de aller fleste. Det er bra at det finnes billigere produkter tilgjengelig, så flere kan få mulighet for behandling. Denne saken handler ikke om biotilsvarende bytte bør gjennomføres eller ikke. Den handler heller ikke om effekt/bivirkninger av originalpreparat kontra biotilsvarende. Den handler om hvordan listene med tilgjengelige TNF/BIO-behandlinger i spesialisthelsetjenesten er utformet, og hvordan det kan ha uheldige utslag for de som ikke er gjennomsnittspasienter. I tillegg kan det føre til at tilliten mellom behandler og pasient blir skadelidende.
Stanger i sykehusveggen
Men først må jeg fortelle bakteppet for at teorien dukket opp. Som pasientorganisasjon med en gratis hjelpetjeneste får vi i Spafo Norge en del henvendelser om dette med behandling og de mulighetene som finnes. Det kan for eksempel handle om usikkerhet i forhold til det å starte på medisin for første gang, bekymring for mulige bivirkninger etc. Det siste halvannet året, cirka, har det kommet mange flere henvendelser om behandling enn normalt. De har tatt kontakt med oss via hjelpetelefonen, e-post, meldinger i sosiale medier, ringt medlemsansvarlig, ringt redaksjonen til medlemsbladet og tatt kontakt med folk i organisasjonen som de kjenner.
- De forteller om fortvilelse og frustrasjon, fordi de opplever mye dårligere effekt av det biotilsvarende produktet de nå får.
- Flere har fått en rekke bivirkninger, mange som ikke er til å leve med.
- De føler de stanger hodet i sykehusveggen, for legene tror ikke på det de forteller. Biotilsvarende medisin regnes som likeverdige, både når det gjelder effekt og bivirkningsprofil. Dermed kan ikke pasientenes erfaring stemme, får de beskjed om.
- Flere forteller at det plutselig sås tvil om diagnosen deres, siden den biotilsvarende varianten ikke fungerer like godt. Derfor tør de ikke gjøre annet enn å fortsette på en medisin som ikke har effekt. Først når det oppstår store/mange bivirkninger har de fått nok. Da er ofte alternativet å være uten behandling istedenfor, siden de ikke får tilbud om andre produkter.
- En forteller at legen sa den manglende effekten dreier seg om placeboeffekten. At det bare er innbilning, fordi hen vet at det er en billigere kopi.
- De forteller om mye dårligere livskvalitet, at de ikke lenger fungerer i arbeid og hverdag, om langtidssykemeldinger og overgang til arbeidsavklaringspenger.
- Noen forteller også at de har gitt opp kampen med sykehuset, og heller har søkt og fått innvilget uføretrygd, selv om ikke alle behandlingsalternativer er forsøkt.
Anonymisert oversikt
Da Spafo Norge hadde orienteringsmøte med Sykehusinnkjøp HF i mars 2025 om TNF/BIO-ordningen, fortalte vi at den økte mengden henvendelser var urovekkende. Vi vet at det vi har fått høre om er kun pasientenes side av saken – deres egne opplevelser og erfaringer. Og det er klart, det er sjelden de som har velfungerende behandling som tar kontakt. I forhold til hvor mange som benytter biologisk medisin i dag, er henvendelsene til oss bare en liten andel, men vi var likevel blitt bekymret.
Sykehusinnkjøp sa de ikke var kjent med mye av det vi fortalte, så de ba oss om å lage en anonymisert oversikt med de tilfellene vi visste om. Dermed startet en ganske omfattende jobb for undertegnede, for å følge opp så mange som mulig av de vi fortsatt hadde dialog med – og kvalitetssikre historiene best mulig. I henhold til GDPR-regelverket har vi ikke anledning til å lagre informasjon om hvem som tar kontakt med oss, uten deres samtykke. Derfor er det en del av henvendelsene til Spafo Hjelper Deg som vi ikke får tatt med i en slik oversikt.
Likepersonsamtaler
Vi loggfører imidlertid aktiviteten til likepersonene våre, blant annet samtaler de har en-til-en fysisk, eller på telefon. I den er det aldri nevnt navn, men noen er flinke og noterer ned hva samtalen dreide seg om. Der fant jeg blant annet:
August 2024:
- Spørsmål om vi visste om andre som hadde dårligere effekt av biotilsvarende medisin, da hen mistet effekt etter 2-3 måneder. Smerter og betennelse tilbake. Bivirkninger som kraftig hodepine og ekstrem svetting, som legen mente bare var overgangsalder. Ville ha råd om hvordan klage på avgjørelsen om å ikke få bytte tilbake til tidligere produkt som virket.
Juni 2024:
- Hjelp til rettigheter og argumentasjon ved tvunget bytte til biologisk medisin med annet virkestoff. Informerte om pasientrettigheter, om mulighet for å klage og bistand via Pasientombudet.
Mai 2024:
- Spørsmål om bytte mellom biologisk medisin med to ulike virkestoff, uten at pasienten hadde vært til time. Fikk kun brev om at det skulle byttes. Bisto med å finne reglene ved bytte mellom ulike virkestoff og at det ikke skal byttes på grunn av kun pris, men gjøres som følge av medisinskfaglig vurdering – i samvalg med pasienten.
April 2024:
- Om biotilsvarende behandling som ikke har effekt på axSpA og alternative muligheter. Hvordan bli tatt på alvor når behandling ikke virker?
Ikke bytte tilbake
Vi spurte også litt rundt i egne revmatikerkretser, om andre hadde hatt lignende erfaringer, og det var det! Jeg ba om lov til å notere ned historiene og fortalte hva det skulle brukes til – inkludert at jeg ønsket å bruke noe av det til artikler i medlemsbladet for å belyse situasjonen.
Felles for flesteparten av samtalene har vært at pasientene har benyttet en biologisk medisin i lengre tid, og har hatt god nytte av den. De får ikke bytte tilbake når det har oppstått problemer med et biotilsvarende produkt, selv om den de hadde før ga god effekt og få bivirkninger.
For ordens skyld; Undertegnede har også kunnet bidra med egen erfaring rundt dette, etter store utfordringer med to biotilsvarende produkter. Det løste seg til slutt, da det ble byttet tilbake til originalpreparatet, som igjen ga god effekt og ingen plagsomme bivirkninger.
Ikke tilgjengelig lenger
De vi har vært i kontakt med forteller om ulike forklaringer de har fått for at det ikke er mulig å bytte tilbake. Ofte har det handlet om originalen av adalimumab (Humira).
- Flere hadde fått beskjed om at det ikke lenger er mulig å forskrive medisinen, da den ikke står på lista over tilgjengelige behandlinger på H-resept for deres diagnose.
- Noen fikk beskjed om at medisinen deres ikke produseres lenger.
- Andre fikk vite at deres medisin ikke lenger tas inn i Norge.
- Noen hadde fått høre at det ikke er lov å skrive ut denne medisinen.
- Noen fikk bare beskjed om at det er umulig, og ingen videre forklaring.
- Noen hadde fått beskjed om at den de hadde før er for dyr, og at det nå er en mye billigere biotilsvarende versjon som alle må benytte.
Lyver de?
Da jeg oppsummerte dette begynte jeg å stusse, for det var overraskende mange som hadde blitt nektet å bytte tilbake til Humira «fordi den ikke lenger var tilgjengelig». Siden jeg har skrevet om disse TNF/BIO-listene hvert år, fra de ble lansert for mange år siden, visste jeg at dette originalproduktet fortsatt var mulig å forskrive. Det koster bare litt mer enn det billigste alternativet, men er inkludert i dokumentet med anbefalinger fra Sykehusinnkjøp for perioden fram til 31. januar 2026.
I starten av dette arbeidet var jeg faktisk ganske sint på pasientenes vegne. Det er jo helt forferdelig om leger lyver til dem, for å slippe å forskrive behandling som koster noe mer.
Men så ble det litt for mange som fortalte noenlunde samme historien. Og jeg har møtt svært mange leger innen revmatologifeltet, både som pasient og redaktør gjennom mange år. De fleste har vært dyktige folk med genuin omtanke for pasientene sine. At så mange skulle snakke usant, eller holde tilbake informasjon om behandlingsmuligheter som finnes, fikk jeg liksom ikke til å stemme.

Eureka!
Så fikk jeg dette Eureka-øyeblikket, da jeg i våres hadde vært på kontroll hos en legespesialist innenfor et annet diagnosefelt. Der ble jeg spurt om hvilke medisiner jeg benyttet nå. Da jeg fortalte at jeg brukte Humira, ble legen veldig overrasket og sa at den ikke var mulig å forskrive lenger. Han hadde jo ingen grunn til å lyve. Vedkommende har ikke ansvar for min biologiske behandling, og jobber ved et helt annet helseforetak.
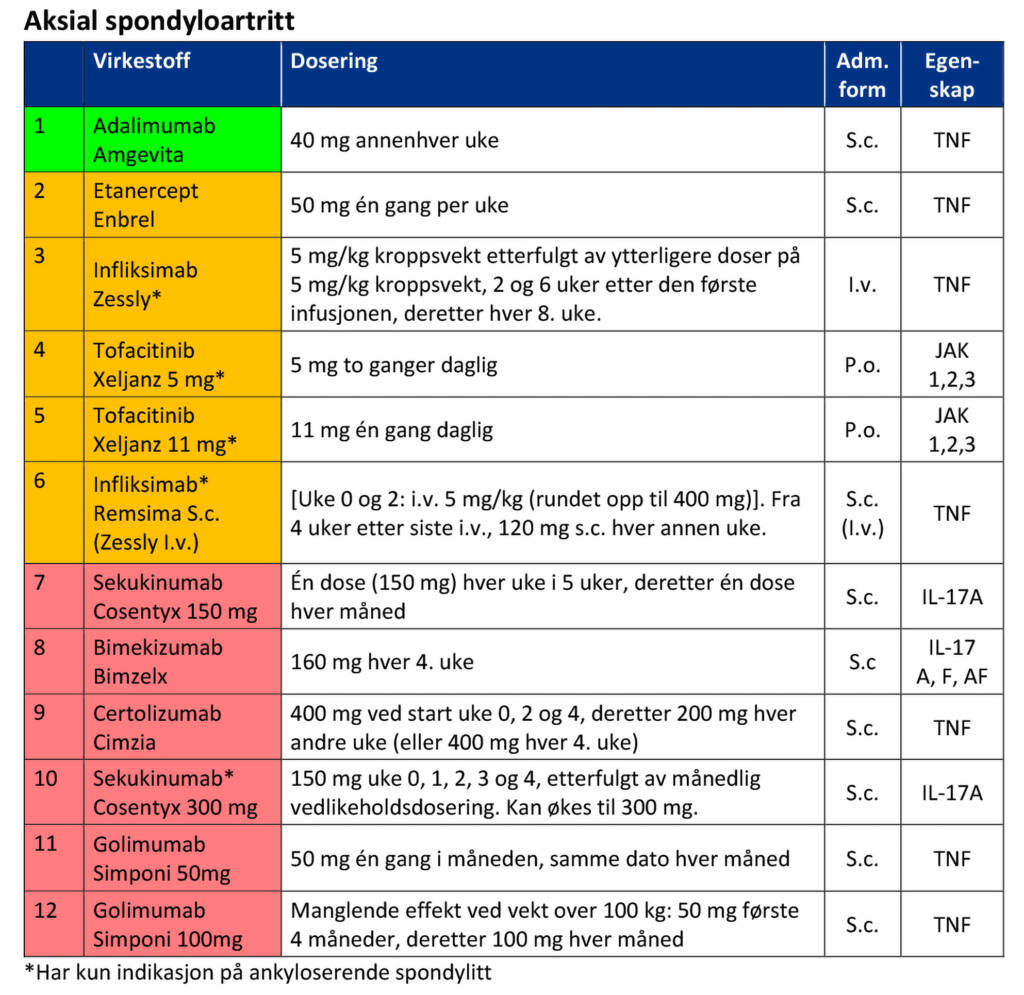
På vei hjem kom jeg på at originalen Humira ikke står oppført på listene under hver enkelt diagnose i TNF/BIO-dokumentet. Den er kun nevnt et stykke ned i tabellen på side 2, der det står forklaring om medisiner med samme virkestoff.
Trafikklys
Etter en anbudsrunde rangeres nemlig de ulike produktene fra billig til dyrest. Siden 2022 har felles praksis ved landets sykehus vært at alle pasienter flyttes over til billigste biotilsvarende produkt, og at det gjøres annethvert år når nye tilbud på biologiske legemidler er hentet inn i en anbudsrunde. Produktene som velges ut blir merket med et fargekodet system, som et trafikklys. Grønt er merket som det fordi det er veldig billig – ikke fordi de grønne er ansett å være mye bedre enn de andre. De produktene som er merket med gult er dyrere alternativer enn det aller billigste. Men det er fortsatt såpass billig at legen på selvstendig grunnlag kan foreta bytte, om det er en medisinsk grunn for det. Det skal bare noteres i pasientens journal hvorfor dette produktet ble valgt. De som har rød bakgrunn er veldig dyre, men fortsatt mulig å forskrive etter at en legegruppe ved sykehuset har diskutert saken og blitt enige.
Leser ikke hele
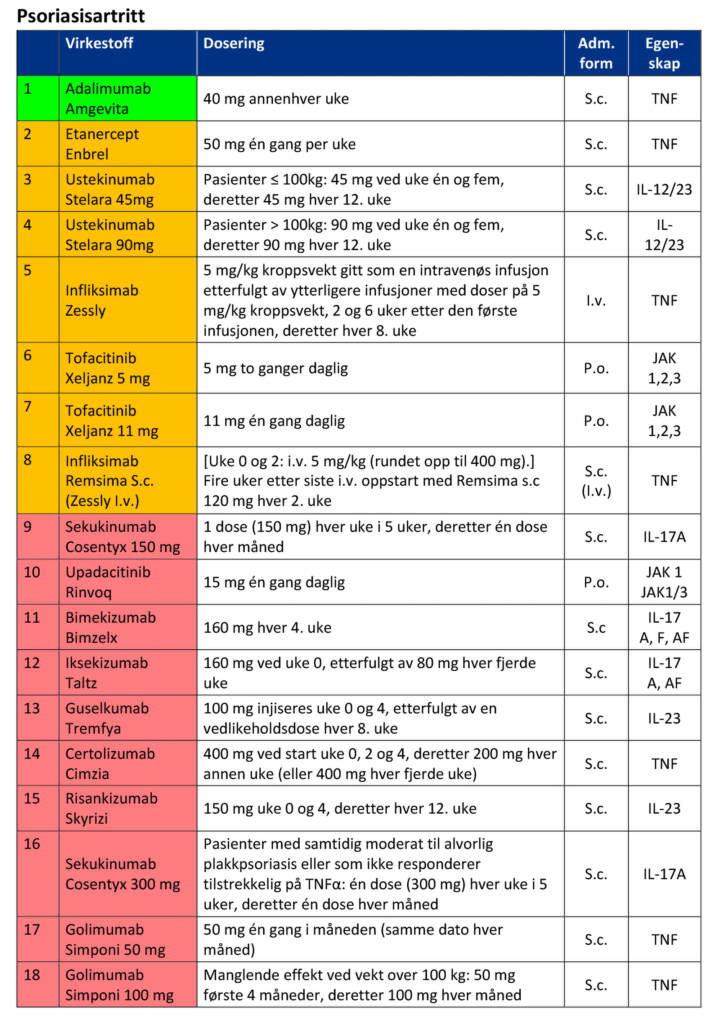
TNF/BIO-dokumentet er utformet med oversiktlige lister for de diagnosene man kan behandle med biologisk medisin. Under hvert diagnosenavn er det laget tabeller, der de legemidlene som kan forskrives ved denne diagnosen er rangert etter fargeskalaen. Om man har en pasient med aksial spondyloartritt blar man derfor rett til side 4 i dokumentet. Om pasienten har psoriasisartritt blar man til side 5. Men der er det per i dag kun Amgevita/Yuflyma som er ført opp med virkestoffet adalimumab, og det er de eneste som er merket med grønt.
Min teori er derfor at i en hektisk sykehushverdag fungerer ikke dokumentet optimalt. For jeg vil anta at få tar seg tid til å lese hele. Derfor får de ikke med seg at det på side 2 er en tabell med produkter med tilsvarende virkestoff og teksten:
«Der Sykehusinnkjøp HF har mottatt tilbud fra flere leverandører på samme virkestoff (biotilsvarende og generika) listes kun rimeligste alternativ i rangeringen per indikasjon.»
Altså at det kun er den billigste varianten av like produkter som er ført inn i listene under hver diagnose. Det er kun i tabellen på side 2 at Humira står oppført som et tilgjengelig alternativ i to styrker – merket med gul bakgrunn. Under er en setning uthevet:
«Valg av produkt med gul bakgrunn skal begrunnes i pasientens journal.»
Rom for forbedring
Så nei, jeg tror ikke at legespesialistene bevisst feilinformerer om tilgjengelige behandlingsmuligheter – fordi det koster mer enn de som er rangert i grønt.
Jeg tror det handler om en misforståelse om hvordan dette dokumentet nå er bygget opp. Før sto nemlig alle alternativene listet opp under hver diagnose, også de med samme virkestoff. Det har etter hvert kommet mange nye behandlingstilbud, og biotilsvarende kopier, så lista ville blitt veldig lang om alle skulle være med under hver diagnose.
Så er spørsmålet hvor bevisst endringen av dokumentet har vært, og hvilke beskjeder som har gått ut til de som skal benytte dokumentet i praksis…
Om min teori stemmer har i hvert fall lista definitivt et forbedringspotensiale, så det kommer tydelig fram ved hver diagnoseoverskrift at det også finnes andre biotilsvarende virkestoff tilgjengelig.
Ingen tilbakemeldinger
Jeg har kontaktet to revmatologer og en hudlege, for å høre hva de tenker om teorien min. I første omgang bare for å snakke litt ‘off the record’ om deres erfaring med dette dokumentet, og om jeg burde jobbe videre med denne saken. Det er tross alt de som vet best hvordan disse listene fungerer i praksis. Jeg har ikke fått respons fra noen av dem. Sykehusinnkjøp har imidlertid svart. Pål Rydstrøm, konstituert avdelingsleder anskaffelser, skriver dette på e-post:
– Anbefalingen er utformet i samarbeid med fagmiljøet, og det skal komme godt frem i den hvilke biotilsvarende legemidler som er tilgjengelige. Sykehusinnkjøp har ikke fått tilbakemeldinger fra klinikere om at anbefalingene er uklare. Dersom vi får slike tilbakemeldinger, vil vi se på dette sammen med klinikerne vi benytter i anskaffelsene.
Humira forsvinner snart
Teksten fram til hit publiserte Spafo Norge i medlemsbladet Spondylitten i september 2025. I skrivende stund, starten av januar 2026, er legespesialistene fortsatt tause. Sykehusinnkjøp har imidlertid publisert listene for hvilke TNF/BIO-produkter som vil være tilgjengelig fra 1. februar 2026 og to år framover.
Der står ikke lenger Humira markert med gult på side 2.
Den er istedenfor flyttet lenger ned på samme side, under oversikten over produkter som ikke skal benyttes, da det ikke er gjort avtale om dem i denne anbudsperioden. Det betyr som regel at legemiddelfirmaene ikke har sendt inn tilbud i anbudskonkurransen. Kostnaden for disse biologiske produktene har dermed ikke noen rabatt, og selges tilsvarer pris i Felleskatalogen. I skrivende stund er kostnaden for en måneds forbruk med 40 mg Humira (adalimumab), penn/sprøyte hver andre uke, 5398 kroner, ifølge Felleskatalogen.
Alle får Hyrimoz
For den kommende anbudsperioden har også flere av de andre biotilsvarende produktene med virkestoffet adalimumab havnet på denne IKKE-lista. To av disse er regnet som de billigste alternativene i inneværende anbudsperiode, Amgevita og Yuflyma.
Fra 1. februar 2026 vil det imidlertid være den biotilsvarende Hyrimoz (adalimumab) som tar over, fordi den da vil være den billigste behandlingen for inflammatorisk sykdom i mage-tarm, hud eller ledd og bløtvev.
Andre TNFalfa-hemmere som er satt på IKKE-lista fra 1. februar 2026 til 31. januar 2028 er Benepali (etanercept) og biotilsvarende Flixabi og Remicade med virkestoffet infliksimab.
Du kan lese mer om hvilke biotilsvarende bytter som vil bli gjort for de som benytter TNFalfa-hemmere i artikkelen vår som heter Nye anbefalinger om biotilsvarende bytter i 2026. Der finner du en tabell over dagens produkter og hvilke biotilsvarende varianter det skal byttes til for de ulike virkestoffene.
Denne artikkelen er hentet fra Spafo Norges medlemsblad Spondylitten. Det er kun en liten andel av artiklene våre som legges ut på nett.
Husk at vi også kan tilby mange gode medlemsfordeler! Klikk her for å finne ut mer om dem
Som medlem kan du velge å lese Spondylitten kun digitalt. Våre medlemmer har tilgang til alle digitale utgaver ved å logge seg inn på MinSide.